|
基因治療是什麼
如果用一把倍率很大的放大鏡看每個人,就可以發現是由一個一個的細胞組成,每個細胞裡面都有成千上萬個被稱為DNA的小片段,DNA就像是電腦的程式碼一樣,不同的程式碼可以讓電腦執行不同的功能,這些具有功能的DNA排列組合就稱為「基因」。如果這些DNA的排列組合出錯,就有可能導致細胞無法發揮正常功能,或是可能突變成癌細胞。
隨著醫療技術的進步,越來越多疾病的源頭都被發現是與調控細胞功能的「基因」有關係,「基因治療」就是找出造成疾病的基因片段或序列,直接從源頭將這個基因做修改或刪除,達到根除疾病的目的。目前可以進行基因治療的疾病以「罕見疾病」及「癌症」兩種類型為主。
基因治療的源起
綜觀藥物發展歷史,由一開始的化學分子藥品、生物製劑到現在廣泛使用的單株抗體蛋白。而隨著次世代基因定序的發展以及藥物製造技術的突破,疾病的治療已經進入「再生醫療」的新世代。藥物發展歷史簡單示意圖如下圖一。
在臺灣,「再生醫療製劑」包含三個種類的藥品:細胞治療製劑、基因治療製劑及組織工程製劑。所以剛剛提到的「基因治療」,在臺灣是屬於再生醫療的其中一種。
其實基因治療並非這幾年才有的概念,早在1953年人類基因的樣子被確定後,就陸續有許多的研究在進行。1989年,美國基因遺傳學教授安德森(William French Anderson),藉由在病人體內植入帶有外來基因的淋巴球,嘗試治療黑色素瘤,但當時並未真正成功治療疾病。隔年,安德森利用基因重組後的反轉錄病毒,治療嚴重複合型免疫缺乏症,此為世界上第一次基因治療的成功案例,安德森也因此被譽為基因療法之父。
所以早在3、40年前,就已經有利用基因治療疾病的概念了,只是由於技術限制,一直未有大量的藥品上市,直到近年來基因定序檢測的發展以及藥品開發的技術突破,才開始有越來越多的藥品進入臨床試驗並且上市。
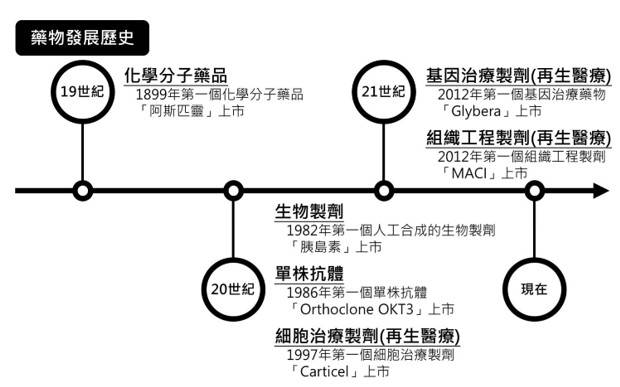 |
圖一、藥物發展歷史示意圖
從最早1899年第一個化學分子合成的藥品「阿斯匹靈」出現之後,藥品從「生物製劑」、「單株抗體(蛋白藥物)」一路發展起來,並且到2000年前後開始有再生醫療製劑出現
|
基因治療製劑的設計
直接修改人體基因並不容易,目前常見的做法是先在實驗室或藥廠裡,合成出一段特定功能的基因,再讓這段基因進到人體裡面去修改細胞的功能。如果直接將合成好的基因注射進身體裡面,不僅有可能跑到錯誤的細胞裡面,也有可能在進入到細胞之前就已經被分解掉了,所以就需要「載體(vector)」這個特殊的設計。
能當作載體的工具有很多,而病毒就是一個常常被拿來當作載體的容器,可將基因放在病毒裡面,再運送到目標細胞內。我們可以將病毒想像成是一輛計程車,基因就坐在這輛車裡面,病毒會依照我們給的地址,將基因載到特定的細胞裡面進行作用。
目前常用來當作載體的病毒是腺病毒(adenovirus)、腺相關病毒(adeno-associated virus,AAV)、慢病毒(lentivirus)。雖然利用病毒傳送聽起來有點可怕,但這些病毒並不會造成人體基因突變,產生感染的危險性也很低,是相對安全的病毒。這種利用病毒當載體的概念,在生物醫學的領域也已經被廣泛使用了,許多常見的疫苗就是利用這個概念製作而成的,因此可以不需要特別擔心。
每個病毒的大小不一樣,所以裡面可以運送的基因數量就不同。另外,每種病毒喜歡到達的器官也不一樣,這種差異稱為「器官親和力」,在設計藥品要選擇哪個病毒的時候,就會參考可以裝的基因數量以及器官親和力,選擇跟疾病親和力較高的病毒。這些病毒對於器官的親和力整理如下表一,打圈代表對於這個器官親和力高。
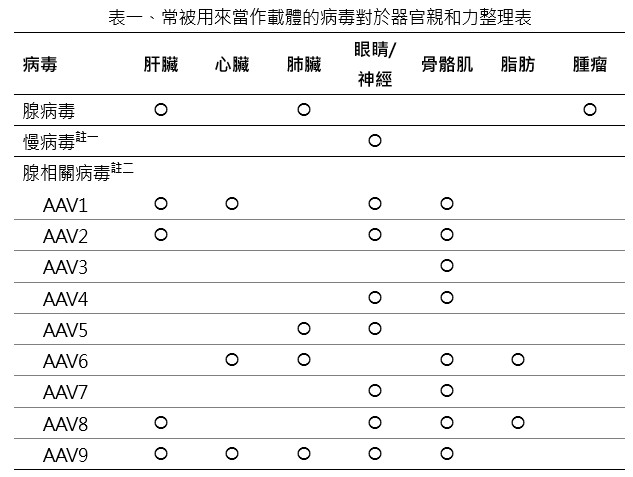 |
註一:慢病毒通常用於體外的細胞改造,如嵌合抗原受體T細胞(Chimeric Antigen Receptor T Cells,CAR-T),因此親和力是對於體外細胞的親和力。
註二:腺相關病毒共有9種血清型(9種兄弟姊妹),分別是AAV1到AAV9。
|
目前臺灣有哪些基因治療藥品
大部分的基因治療藥物都還在臨床試驗階段,依照衛生福利部的資料,截至2024年4月為止,臺灣有46件基因治療臨床試驗(治療的疾病主要是罕見疾病及癌症兩種)以及103件細胞治療臨床試驗(治療的疾病主要是癌症、神經及心血管疾病三種)在進行中。而目前則有4個再生醫療製劑已經在臺灣上市了,藥品名稱及可以治療的疾病整理如下表二:
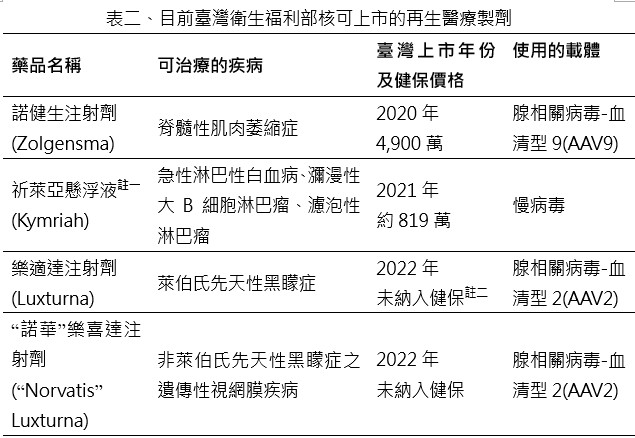 |
註一:祈萊亞懸浮液屬於嵌合抗原受體T細胞(Chimeric Antigen Receptor T Cells,CAR-T)產品,是先將免疫細胞透過抽血等方式從人體分離出來,利用病毒在體外先改造免疫細胞,使其更能鎖定癌症細胞後,再將改造後的免疫細胞輸進人體內消滅癌細胞,因此同時具有再生醫療規範內的「基因治療製劑」以及「細胞治療製劑」的特性。
註二:樂適達注射劑在臺灣還未納入健保,在美國單隻眼睛治療費用為42.5萬美元(約1,395萬台幣);雙眼治療費用為85萬美元(約2,790萬台幣)。
|
由於基因治療藥物製造技術上的要求,這類藥品售價都非常昂貴,以諾健生注射劑為例,這個藥品2020年在臺灣上市使用,2023年8月被納入健保給付,是第一個被納入臺灣健保的基因治療藥品,每支售價高達4,900萬,雖然售價非常驚人,但這類藥品由於是針對基因直接作用,理論上施打一次可以終身有效,不過也同時存在治療失敗而沒有效果的風險。
結語:
臺灣在2015年發生了八仙塵暴事件,大量燒燙傷患者需要進行人工植皮,衛生福利部因此專案進口日本已上市的自體皮膚細胞培養產品(autologous cultured epidermis,JACE),但是當時也發現臺灣缺乏再生醫療產品的管理法規,因此八仙塵暴事件之後政府開始重視這個問題,再加上後來癌症病友的爭取,因而催生出後來的「再生醫療法」以及「再生醫療製劑管理條例」(合稱「再生醫療雙法」)。
這兩個法案已在2024年6月立法院三讀通過,相信「再生醫療雙法」的上路,會對未來這些藥品的發展與上市有更大的助益。
目前這些藥品的售價都非常昂貴,施打一次需要的花費都是千萬以上,並非一般民眾可以負擔的價格,在疾病、售價與效果三者之間的考量,就需要醫師與病人本身經過充分溝通與討論之後再做決定。
資料來源:
- Rosenberg SA, Aebersold P, Cornetta K, et al. Gene transfer into humans immunotherapy of patients with advanced melanoma, using tumor infiltrating lymphocytes modified by retroviral gene transduction. N Engl J Med. 1990;323(9):570 578.
- Anderson WF, Blaese RM, Culver K. The ADA human gene therapy clinical protocol: Points to Consider response with clinical protocol, July 6, 1990. Hum Gene Ther. 1990;1(3):331 362.
- Ginn SL, Amaya AK, Alexander IE, Edelstein M, Abedi MR. Gene therapy clinical trials worldwide to 2017: An update. J Gene Med. 2018 May;20(5):e3015.
- Flomenberg, P., & Daniel, R. (2024). Overview of gene therapy, gene editing, and gene silencing. UpToDate, Waltham, MA (Accessed on Dec 29, 2024)
- Henderson, M. L., Zieba, J. K., Li, X., Campbell, D. B., Williams, M. R., Vogt, D. L., Bupp, C. P., Edgerly, Y. M., Rajasekaran, S., Hartog, N. L., Prokop, J. W., & Krueger, J. M. (2024). Gene Therapy for Genetic Syndromes: Understanding the Current State to Guide Future Care. Biotech (Basel (Switzerland)), 13(1), 1.
- 再生醫療製劑條例及我國核准現況,衛生福利部食品藥物管理署藥品組,2024年7月2日。(衛生福利部食品藥物管理署,業務專區>藥品>再生醫療製劑管理專區>再生醫療製劑相關演講https://www.fda.gov.tw/TC/siteList.aspx?sid=12080,最後瀏覽日:2024年12月29日)
- Nayerossadat, N., Maedeh, T., & Ali, P. A. (2012). Viral and nonviral delivery systems for gene delivery. Advanced biomedical research, 1, 27.
- Service of Adeno-associated Viral Vectors (AAV),中央研究院(https://www.ibms.sinica.edu.tw/aav/index.html,最後瀏覽日:2024年12月29日)
- Issa, S. S., Shaimardanova, A. A., Solovyeva, V. V., & Rizvanov, A. A. (2023). Various AAV Serotypes and Their Applications in Gene Therapy: An Overview. Cells, 12(5), 785.
- Pillay, S., Zou, W., Cheng, F., Puschnik, A. S., Meyer, N. L., Ganaie, S. S., Deng, X., Wosen, J. E., Davulcu, O., Yan, Z., Engelhardt, J. F., Brown, K. E., Chapman, M. S., Qiu, J., & Carette, J. E. (2017). Adeno-associated Virus (AAV) Serotypes Have Distinctive Interactions with Domains of the Cellular AAV Receptor. Journal of virology, 91(18), e00391-17.
|